Clinical efficacy analysis of radical nephrectomy combined with lymph node dissection for 93 patients with locally advanced stage pN1 renal carcinoma in a single center
-
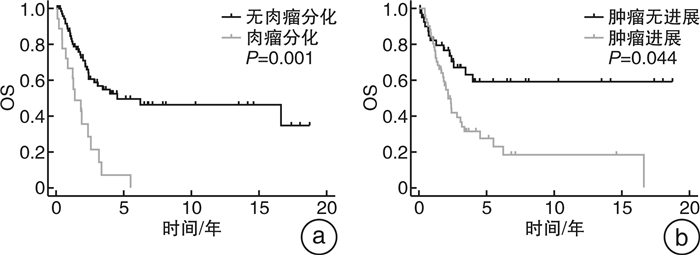
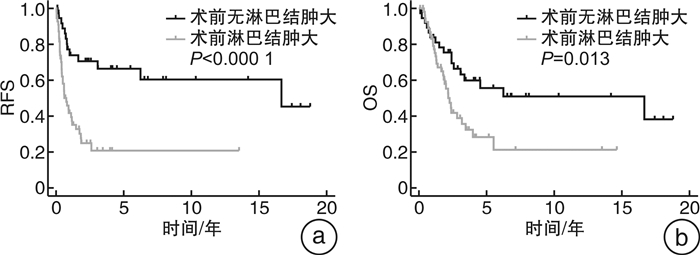
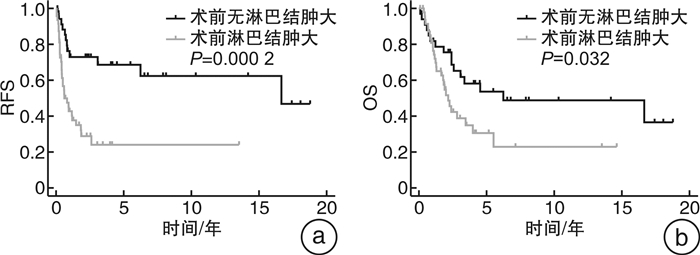
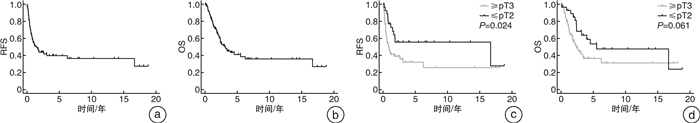
摘要: 目的 探讨pN1期局部进展性肾癌行根治性肾切除术联合区域淋巴结清扫术的临床疗效。方法 收集1999年3月—2022年2月于中山大学肿瘤防治中心泌尿外科行根治性肾切除术后病理为pN1期的局部进展性肾癌患者的临床资料。应用单因素/多因素logistic回归和Kaplan-Meier生存曲线对临床数据进行分析。结果 93例pT1~4N1M0期肾癌患者,男62例,女31例,平均年龄为(47±16)岁。pT1~2期肾癌患者28例,pT3期及以上65例。术中中位清扫淋巴结数目为8.0(4.0,12.0)个,术后病理淋巴结转移中位数目为2.0(1.0,5.0)个。随访过程中51例患者出现术后肿瘤进展,其中局部复发7例,远处转移44例。中位无复发生存期(relapse free survival,RFS)为0.87(0.35,2.60)年,中位总生存时间(overall survival,OS)为2.17(1.13,4.11)年,其中1、3和5年RFS率分别为46.2%、23.7%和14.0%;1、3和5年的OS率分别为80.6%、38.7%和19.3%。肉瘤样分化和术后复发转移是生存预后的独立危险因素(P=0.003,P=0.001);术前淋巴结肿大是肾癌术后远处转移的独立危险因素(P=0.044);多组区域淋巴结转移是肾癌术后局部复发的独立危险因素(P=0.036)。结论 局部进展性肾癌伴淋巴结转移的患者术后复发转移概率高,预后差,需要密切监测随访。术前区域淋巴结肿大、原发灶肉瘤样变以及术后肿瘤进展是pN1期进展性肾癌的不良预后因素。Abstract: Objective To assess the clinical effectiveness of radical nephrectomy combined with regional lymphadenectomy in treating locally advanced renal carcinoma at pathological N1 stage.Methods Clinical data from a cohort comprising ninety-three patients diagnosed with locally advanced renal carcinoma at pathological N1 stage who underwent radical nephrectomy at Sun Yat-sen Cancer Center from March 1999 to February 2022 were retrospectively collected for analysis by using univariate/multivariate logistic regression models as well as Kaplan-Meier survival curves.Results A total of 93 patients diagnosed with pT1-4N1M0 renal carcinoma had a mean age of (47±16) years and a male-to-female ratio of 62∶31. There were 28 patients diagnosed with stage pT1-2 renal cancer, while 65 patients had advanced stages of pT3 and above. The median number of lymph nodes dissected during operation was 8.0(4.0, 12.0), and the median number of pathological lymph node metastases after operation was 2.0(1.0, 5.0). During the follow-up period, tumor progression occurred in 51 patients, including local recurrence in 7 cases and distant metastasis in 44 cases. The median relapse-free survival(RFS) was approximately 0.87 years(range from 0.35 to 2.60 years), while the median overall survival(OS) was approximately equal to 2.17 years(range from 1.13 to 4.11 years). The 1, 3 and 5-year RFS rates were 46.2%, 23.7% and 14.0%, respectively. The 1, 3 and 5-year OS rates were 80.6%, 38.7% and 19.3%, respectively.Sarcomatoid differentiation, postoperative tumor progression were identified as independent risk factors in prognosis (P=0.003, P=0.001). Preoperative lymph node enlargement was an independent risk factor in postoperative distant metastasis (P=0.044), and multi-group regional lymph node metastases were independent risk factors in postoperative local recurrence (P=0.036).Conclusion Lymph node-metastatic locally advanced renal carcinoma shows a high likelihood of postoperative recurrence and metastasis and poor postoperative prognosis, and thus requires intensive monitoring and follow-up. Preoperative regional lymph node enlargement, sarcomatoid differentiation, as well as postoperative tumor progression are significant adverse prognostic factors for stage N1 progressive renal carcinoma.
-
Key words:
- locally advanced renal carcinoma /
- lymph node enlargement /
- tumor progression /
- prognosis
-

-
表 1 93例患者基本资料
例(%),X±S,M(Q1,Q3) 项目 数值 项目 数值 年龄/岁 47±16 术后 BMI/(kg/m2) 22.1±3.7 局部复发 7(7.5) 性别 远处转移 44(47.3) 男 62(66.7) 并发症(Clavien分级) 女 31(33.3) Ⅱ级 3(3.2) 症状 Ⅲ级 1(1.1) 无症状 30(32.2) T分期 血尿 35(37.7) ≤pT2 28(30.1) 腰部胀痛 17(18.3) ≥pT3 65(69.9) 其他不适 11(11.8) 病理类型 手术方式 透明肾细胞癌 37(39.8) 开放 79(84.9) 乳头状肾细胞癌 21(22.6) 腹腔镜 9(9.7) 嫌色肾细胞癌 3(3.2) 机器人 5(5.4) 其他类型 32(34.4) 肿瘤位置 清扫淋巴结数目/个 8.0(4.0,12.0) 左侧 49(52.7) 淋巴结阳性/个 2.0(1.0,5.0) 右侧 44(47.3) 脉管内癌栓 42(45.2) 肿瘤最大直径/cm 7.5(5.3,10.0) 肿瘤坏死 50(53.8) 肉瘤样分化 18(19.3) 表 2 术后总生存时间的单因素/多因素logistic回归分析
例(%),M(Q1,Q3) 因素 生存(44例) 死亡(49例) |Z| 单因素P值 |Z| 多因素P值 肿瘤位置 0.755 0.450 左 24(54.5) 25(51.0) 右 20(45.5) 24(49.0) 血尿 1.094 0.274 是 14(31.8) 21(42.9) 否 30(68.2) 28(57.1) 术后肿瘤进展 3.315 0.001 3.288 0.001 是 13(29.5) 31(63.3) 否 31(70.5) 18(36.7) T分期 0.792 0.428 ≤pT2 15(34.1) 13(26.5) ≥pT3 29(65.9) 36(73.5) 术前淋巴结肿大 1.272 0.203 是 23(52.3) 32(65.3) 否 21(47.7) 17(34.7) 淋巴结转移数目/个 2.0(1.0,5.8) 3.0(1.0,5.0) 0.216 0.829 多组区域淋巴结转移 0.972 0.331 是 12(27.3) 18(36.7) 否 32(72.7) 31(63.3) 多个区域淋巴结转移 1.888 0.059 是 23(52.3) 35(71.4) 否 21(47.7) 14(28.6) 肿瘤最大直径/cm 8.0(5.0,10.9) 7.0(5.5,9.7) 0.726 0.468 脉管内癌栓 1.195 0.232 是 17(38.6) 25(51.0) 否 27(61.4) 24(49.0) 肿瘤坏死 0.143 0.886 是 24(54.5) 26(53.1) 否 20(45.5) 23(46.9) 肉瘤样分化 2.955 0.003 3.012 0.003 是 2(4.5) 16(32.7) 否 42(95.5) 33(67.3) 表 3 术后肿瘤进展单因素/多因素logistic回归分析
例(%),M(Q1,Q3) 因素 肿瘤进展(51例) 肿瘤无进展(42例) |Z| 单因素P值 |Z| 多因素P值 肿瘤位置 0.780 0.435 左 25(49.0) 24(57.1) 右 26(51.0) 18(42.9) 血尿 0.776 0.438 是 21(41.2) 14(33.3) 否 30(48.8) 28(66.7) 透明细胞癌 0.549 0.583 是 19(37.3) 18(42.9) 否 32(62.7) 24(57.1) 肿瘤最大直径/cm 7.0(6.0,9.3) 7.8(4.0,11.0) 0.074 0.942 T分期 1.513 0.130 ≤pT2 12(23.5) 16(38.1) ≥pT3 39(76.5) 26(61.9) 术前淋巴结肿大 3.244 0.001 2.195 0.028 是 38(74.5) 17(40.5) 否 13(25.5) 25(59.5) 淋巴结转移数目/个 3.0(1.0,6.0) 2.0(1.0,4.0) 0.837 0.402 多组区域淋巴结转移 2.822 0.005 1.598 0.110 是 23(45.1) 7(16.7) 否 28(54.9) 35(83.3) 多个区域淋巴结转移 0.942 0.346 是 34(66.7) 24(57.1) 否 17(33.3) 18(42.9) 脉管内癌栓 0.014 0.989 是 23(45.1) 19(45.2) 否 28(54.9) 23(54.8) 肿瘤坏死 0.242 0.808 是 23(45.1) 22(52.4) 否 28(54.9) 20(47.6) 肉瘤样分化 0.594 0.553 是 11(21.6) 7(16.7) 否 40(78.4) 35(83.3) 表 4 术后肿瘤远处转移单因素/多因素logistic回归分析
例(%),M(Q1,Q3) 因素 转移(44例) 无转移(42例) |Z| 单因素P值 |Z| 多因素P值 肿瘤位置 1.081 0.276 左 20(45.5) 24(57.1) 右 24(54.5) 18(42.9) 血尿 0.726 0.468 是 18(40.9) 14(33.3) 否 26(59.1) 28(66.7) 透明细胞癌 0.030 0.976 是 19(43.2) 18(42.9) 否 25(56.8) 24(57.1) 肿瘤最大直径/cm 8.0(6.0,10.0) 7.8(5.0,11.0) 0.357 0.721 T分期 1.779 0.075 ≤pT2 9(20.5) 16(38.1) ≥pT3 35(79.5) 26(61.9) 术前淋巴结肿大 2.958 0.003 2.018 0.044 是 32(72.7) 17(40.5) 否 12(27.3) 25(59.5) 淋巴结转移数目/个 2.0(1.0,5.0) 2.0(1.0,4.0) 0.507 0.612 多组区域淋巴结转移 2.600 0.009 1.482 0.138 是 19(43.2) 7(16.7) 否 25(46.8) 35(83.3) 多个区域淋巴结转移 0.615 0.539 是 28(63.6) 24(57.1) 否 16(36.4) 18(42.9) 脉管内癌栓 0.231 0.817 是 21(47.7) 19(45.2) 否 23(52.3) 23(54.8) 肿瘤坏死 0.413 0.680 是 25(56.8) 22(52.4) 否 19(43.2) 20(47.6) 肉瘤样分化 0.185 0.853 是 8(18.2) 7(16.7) 否 36(81.8) 35(83.3) 术后辅助治疗 1.483 0.138 是 8(18.2) 3(7.1) 否 36(81.8) 39(92.9) 表 5 术后肿瘤局部复发单因素/多因素分析
例(%),M(Q1,Q3) 因素 局部复发(7例) 无复发(42例) |Z| 单因素P值 |Z| 多因素P值 肿瘤最大直径/cm 6.6(5.0,7.0) 7.8(5.0,11.0) 0.919 0.358 T分期 0.239 0.811 ≤pT2 3(42.9) 16(38.1) ≥pT3 4(57.1) 26(61.9) 术前淋巴结肿大 1.936 0.053 是 6(85.7) 17(40.5) 否 1(14.3) 25(59.5) 淋巴结转移数目/个 6.0(2.0,10.0) 2.0(1.0,4.0) 1.217 0.224 多组区域淋巴结转移 2.184 0.029 2.088 0.036 是 4(57.1) 7(16.7) 否 3(42.9) 35(83.3) 多个区域淋巴结转移 1.338 0.181 是 6(85.7) 24(57.1) 否 1(14.3) 18(42.9) 脉管内癌栓 0.813 0.416 是 2(28.6) 19(45.2) 否 5(71.4) 23(54.8) 肿瘤坏死 0.465 0.642 是 3(42.9) 22(52.4) 否 4(57.1) 20(47.6) 肉瘤样分化 1.521 0.128 1.367 0.172 是 3(42.9) 7(16.7) 否 4(57.1) 35(83.3) -
[1] Wang ZP, Wang L, Wang S, et al. Burden of kidney cancer and attributed risk factors in China from 1990 to 2019[J]. Front Public Health, 2022, 10: 1062504. doi: 10.3389/fpubh.2022.1062504
[2] 侯乃侨, 翟炜, 郑军华. 显微知著: 人工智能在肾癌数字病理中的应用现状及挑战[J]. 中国癌症防治杂志, 2024, 16(2): 143-151.
[3] 韩雪阳, 高瞻, 刘勇. 术前全身炎症反应指数和纤维蛋白原在肾癌切除术后肿瘤预后的影响[J]. 临床泌尿外科杂志, 2021, 36(7): 567-572. https://lcmw.whuhzzs.com/article/doi/10.13201/j.issn.1001-1420.2021.07.012
[4] Capitanio U, Leibovich BC. The rationale and the role of lymph node dissection in renal cell carcinoma[J]. World J Urol, 2017, 35(4): 497-506. doi: 10.1007/s00345-016-1886-3
[5] Ljungberg B, Albiges L, Abu-Ghanem Y, et al. European association of urology guidelines on renal cell carcinoma: the 2022 update[J]. Eur Urol, 2022, 82(4): 399-410. doi: 10.1016/j.eururo.2022.03.006
[6] Campbell SC, Clark PE, Chang SS, et al. Renal mass and localized renal cancer: evaluation, management, and follow-up: AUA guideline: part I[J]. J Urol, 2021, 206(2): 199-208. doi: 10.1097/JU.0000000000001911
[7] 陈旭, 尚攀峰. 局限性肾癌术后复发与手术相关因素的研究进展[J]. 中国微创外科杂志, 2022, 22(11): 903-908. doi: 10.3969/j.issn.1009-6604.2022.11.012
[8] Eisenhauer EA, Therasse P, Bogaerts J, et al. New response evaluation criteria in solid tumours: revised RECIST guideline(version 1.1)[J]. Eur J Cancer, 2009, 45(2): 228-247. doi: 10.1016/j.ejca.2008.10.026
[9] Escudier B, Porta C, Schmidinger M, et al. Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2019, 30(5): 706-720. doi: 10.1093/annonc/mdz056
[10] 肖若陶, 徐楚潇, 陆敏, 等. 肉瘤样肾癌34例临床病理特征及预后分析[J]. 现代泌尿外科杂志, 2021, 26(6): 481-484, 518. doi: 10.3969/j.issn.1009-8291.2021.06.007
[11] 黄庆波, 马鑫, 张旭. 晚期肾癌的转移机制及治疗方式[J]. 微创泌尿外科杂志, 2015, 4(1): 58-62.
[12] 芮晨宇, 樊伟林, 孙巍, 等. 基于CT影像学参数探讨肾周脂肪对肾癌诊断与预后判断的临床意义[J]. 临床泌尿外科杂志, 2023, 38(12): 929-933. https://lcmw.whuhzzs.com/article/doi/10.13201/j.issn.1001-1420.2023.12.008
[13] Blom JHM, van Poppel H, Maréchal JM, et al. Radical nephrectomy with and without lymph-node dissection: final results of European organization for research and treatment of cancer(EORTC)randomized phase 3 trial 30881[J]. Eur Urol, 2009, 55(1): 28-34. doi: 10.1016/j.eururo.2008.09.052
[14] Rosiello G, Palumbo C, Knipper S, et al. Histotype predicts the rate of lymph node invasion at nephrectomy in patients with nonmetastatic renal cell carcinoma[J]. Urol Oncol, 2020, 38(5): 537-544. doi: 10.1016/j.urolonc.2020.01.013
[15] Bhindi B, Wallis CJD, Boorjian SA, et al. The role of lymph node dissection in the management of renal cell carcinoma: a systematic review and meta-analysis[J]. BJU Int, 2018, 121(5): 684-698. doi: 10.1111/bju.14127
[16] Farber NJ, Rivera-Núñez Z, Kim S, et al. Trends and outcomes of lymphadenectomy for nonmetastatic renal cell carcinoma: a propensity score-weighted analysis of the national cancer database[J]. Urol Oncol, 2019, 37(1): 26-32. doi: 10.1016/j.urolonc.2018.10.004
[17] Whitson JM, Harris CR, Reese AC, et al. Lymphadenectomy improves survival of patients with renal cell carcinoma and nodal metastases[J]. J Urol, 2011, 185(5): 1615-1620. doi: 10.1016/j.juro.2010.12.053
[18] 李飞, 问晓东, 柴红强, 等. 局部进展期肾癌患者术后预后列线图的建立与验证[J]. 现代泌尿外科杂志, 2024, 29(4): 334-341.
[19] Kuusk T, Brouwer O, Graafland N, et al. Sentinel lymph node biopsy in renal tumors: surgical technique and safety[J]. Urology, 2019, 130: 186-190. doi: 10.1016/j.urology.2019.04.026
[20] 魏梦超, 石冰冰, 邢宝坤. 肾癌综合诊治的研究进展[J]. 北京医学, 2023, 45(7): 618-622.
[21] Motzer RJ, Ravaud A, Patard JJ, et al. Adjuvant sunitinib for high-risk renal cell carcinoma after nephrectomy: subgroup analyses and updated overall survival results[J]. Eur Urol, 2018, 73(1): 62-68. doi: 10.1016/j.eururo.2017.09.008
[22] Choueiri TK, Tomczak P, Park SH, et al. Adjuvant pembrolizumab after nephrectomy in renal-cell carcinoma[J]. N Engl J Med, 2021, 385(8): 683-694. doi: 10.1056/NEJMoa2106391
[23] Gu LY, Peng C, Li HK, et al. Neoadjuvant therapy in renal cell carcinoma with tumor thrombus: a systematic review and meta-analysis[J]. Crit Rev Oncol Hematol, 2024, 196: 104316.
-




 下载:
下载: